https://www.vitalstoff-lexikon.de/Spurenelemente/Kupfer/Funktionen
Caeruloplasmin
Caeruloplasmin ist ein einkettiges alpha-2-Globulin mit einem Kohlenhydratanteil von 7 %. Ein einziges Caeruloplasmin-Molekül enthält sechs Kupferatome, die in biologischen Systemen überwiegend in ihrer 2-wertigen Form vorliegen und für die oxidative Funktion des Enzyms im pH-Bereich 5,4-5,9 essentiell sind [5, 6].
Caeruloplasmin weist mehrere Funktionen auf: Als
Bindungs- und Transportprotein enthält Caeruloplasmin 80-95 % des Plasmakupfers und verteilt dieses bedarfsgerecht an verschiedene Gewebe und Organe. Zudem ist es am Transport von
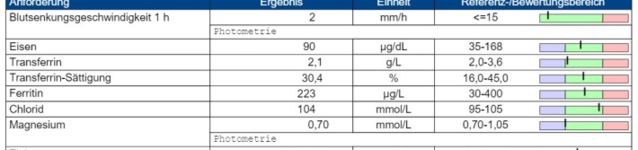
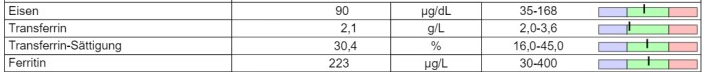
Eisen (Fe) und
Mangan (Mn) im Blutplasma beteiligt.
Durch die Bindung freier Kupfer-, Eisen- und Mangan-Ionen verhindert Caeruloplasmin die Bildung freier Radikale. Letztere stellen hochreaktive Sauerstoffmoleküle oder organische Verbindungen, die Sauerstoff enthalten, wie Superoxid, Hyperoxid oder Hydroxyl, dar. In freier Form sind sowohl Kupfer, Eisen als auch Mangan sehr aggressive Elemente, die prooxidativ wirken. Sie sind bestrebt, einem Atom oder Molekül Elektronen zu entreißen, wodurch freie Radikale entstehen, die wiederum anderen Substanzen ebenfalls Elektronen entziehen. So kommt es in einer Kettenreaktion zur stetigen Vermehrung der Radikale im Körper –
oxidativer Stress. Freie Radikale sind in der Lage, unter anderem Nukleinsäuren – DNA und RNA –, Proteine, Lipide und Fettsäuren, Kollagen, Elastin sowie Blutgefäße zu schädigen. Infolge der Cu-, Fe- und
Mn-Bindung verhindert Caeruloplasmin solche oxidativen Zell- und Gefäßschäden [4, 5, 6, 28].
Des Weiteren weist Caeruloplasmin enzymatische Funktionen auf.
Es katalysiert multiple Oxidationsreaktionen und ist dadurch im Eisenstoffwechsel involviert. Caeruloplasmin wird aus diesem Grund auch als
Ferroxidase I bezeichnet. Seine wesentliche Aufgabe besteht darin, das Spurenelement
Eisen von seiner 2-wertigen (Fe2+) in seine 3-wertige Form (Fe3+) umzuwandeln. Das im Enzym enthaltende Kupfer entzieht dazu dem Eisen Elektronen und nimmt diese auf, wodurch es selbst seine Oxidationsstufe von Cu2+ zu Cu+ wechselt.
Durch die
Oxidation von Eisen ermöglicht Caeruloplasmin die
Bindung von Fe3+ an Plasmatransferrin, einem Transportprotein, das für die Eisenversorgung der Körperzellen verantwortlich ist. Nur in Form von Fe-Transferrin kann Eisen zu den Erythrozyten (rote Blutkörperchen) beziehungsweise Zellen – gelangen und dort für die
Hämoglobinsynthese verfügbar gemacht werden. Hämoglobin ist der eisenhaltige, rote Blutfarbstoff der Erythrozyten (rote Blutkörperchen).
Die Tatsache, dass der Eisentransport zu den Körperzellen, insbesondere zu den Erythrozyten durch Kupfermangel beeinträchtigt wird, zeigt die Bedeutung des Caeruloplasmins und dessen Funktion. Schließlich sind der Eisen- und Kupferstoffwechsel eng miteinander verknüpft [6, 13, 14, 16, 17, 21, 22, 25, 28].