nullzero
Temporär gesperrt
Themenstarter
- Beitritt
- 13.08.16
- Beiträge
- 784
Sowohl das Halbmetall Arsen als auch der Mineralstoff Phosphat sind Bestandteile unserer Erde. Sie sind sogar notwendig zu unserem Leben.
Über diese Phosphate wird ADP produziert und wenn es wirklich zutreffen sollte, dass der Arsenstoffwechsel uns vor gewissen Keimen schützt, wie Dr. Trarello mit seiner Arsentherapie beschreibt, dann finde ich das ist Bemerkenswert und zu beachten.
Das sage ich weil ich mir sicher bin, dass es Erreger gibt die in diesem Giftigen Umfeld sich aufhalten bzw. dieses Giftige Umfeld zu Ihrem Schutz aufbauen. Siehe dazu das Thema Muskelschmerzen oder bei mir noch diese Rückenschmerzen.
Der Stoffwechsel und die Methylisierung in den Pflanzen und in unserem Körper ist eigentlich geregelt. Mit geregelt meine ich, dass auch die Entgiftung dieser Stoffe geregelt von statten geht, wenn diese Stoffe dem natürlichen Ursprung entsprechen.
Das Zeigen die Anhänge.
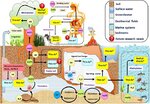
- Arsen im Grundwasser
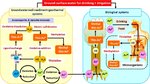
- Arsen-Methylisierung
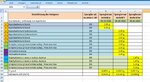
- Arsen Bakterien
Gerade die Liste Arsen Bakterien finde ich doch sehr interessant und wichtig. Da doch gerade dort mehrere meiner pathogenen Keime aufgeführt sind. Und ich weis durch lesen im Forum, dass z.B. viele über Beschwerden und dann Klebsiella oxytoca genannt haben. Einen Bezug zum Candida-Pilz oder Galabrata wäre abzuklären, da ja Pilze Schwermetalle anziehen.
Durch die chemische Veränderung manipulieren wir jedoch diese Vorgänge und die Methylisierung läuft fehl.
Was mich jetzt einfach ganz gewaltig stört, dass ich feststellen musste, ich bin wohl nicht alleine von dem Erkrankungsproblem betroffen. Deswegen habe ich nie aufgebene danach zu suchen.
Ich hab auch bisher immer versucht alle ärztlichen Möglichkeiten zu nutzen, dass mir vielleicht jemand gesagt hätte, sie haben einen Gendefekt. Aber wie der Ablauf der Genberatung an der Uni Ulm verlaufen war und durchgeführt wurde, es war ein Witz sowohl personell von dem Arzt als auch Thematisch das Ergebnis. Okay wenn ich den Gendefekt kenne, oder ich weis das gibt es ein bestimmtes Phosphatproblem dann weis man das und befasst sich damit, was ist dazu bekannt, wie kann und muss ich mich verhalten bei der Ernährung, was sollte ich vermieden usw..
Aber so wie jetzt stellt sich ja keine Lösung dar. Es kann sein der Enzym-Schalter ist irreparabel geschädigt oder er ist reparabel vielleicht temporär. Sind die Keime, der Biofilm als Ursache zu sehen oder die Nahrungsmittel und welche. Ist die unterstützende Entgiftung nützlich oder produziert der Körper weiter immer weiter Arsen und lagert dieses ein.
Dazu sollte doch die Medizin da sein, mich in der Frage zu unterstützen. Muss ich denn deshalb Jahre im Internet danach suchen und mir den Ärger mit den Ärzten haben, weil ich vielleicht einen Ansatz im Arztgespräch einbringe.
Oder muss ich hunderte Nahrungsmittel und die sich ständig verändernden Herstellungsprodukte durchtesten, nur um mich ernähren zu können. Es muss doch festzustellen sein, welches Phosphat/e ob chemisch, natürlich oder in Kombination mit Keimen diesen Fehler verursachen.
Nun musste ich feststellen, dass dieses Enzym-Hemmung von Glyceraldehyd-3-phosphatdehydrogenase (GAPDH) durch Schwermetalle bzw. Arsen zwar bekannt ist, aber es keine Prüfung in der medizinischen Diagnostik gibt. Jedenfalls habe ich noch nichts gefunden. Im EBM-Katalog ist es nicht als Parameter zur Abrechnung erfasst.
Die Umweltmedizin prüft bzw. kann die Stoffwechselstörung das Schlüsselenzym Glucose-6-phosphat-dehydrogenase überprüfen, denn die Zellen brauchen NADPH/H+. Mit Vitamin C könnte man hier Einfluss nehmen.
Deshalb, wieso sollte ich jetzt viel Geld ausgeben für eine Behandlung die die Ursache nicht trifft. Diese 50:50 ärztlichen Behandlungen stellen mich nicht zufrieden.
Will mal noch zwei Beiträge zum Thema Arsen in Abstracten-Form einbringen.
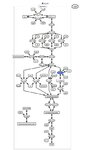
Glykolyse und Pyruvatoxidation
https://www.sciencedirect.com/science/article/pii/B9780323074469000064
Arsenat- und Arsenitvergiftung
Arsenatvergiftung ist auf die Entkopplung der Phosphorylierung auf Substratebene durch G3P-Dehydrogenase zurückzuführen. Arsenat ist ein strukturelles Analogon des Phosphats und wird in 3PG eingebaut, um ein instabiles gemischtes Anhydrid zu bilden. Das Endergebnis ist die Freisetzung von Arsenat ohne Bildung von ATP. Dadurch wird der Nettogewinn von ATP durch anaerobe Glykolyse eliminiert und ist daher für den RBC am schädlichsten.
Aerobe Zellen sind betroffen, wenn Arsenat während der oxidativen Phosphorylierung mit der anschließenden spontanen Hydrolyse in ATP eingebaut wird, um ADP und freies Arsenat zu erzeugen. In beiden Fällen wird auch die mit der ATP-Hydrolyse verbundene Wärme freigesetzt.
Arsenitvergiftung ist auf die kovalente Reaktion von Arsenit mit Liponsäure zurückzuführen, wodurch verhindert wird, dass die Hydroxyethylgruppe von Thiamin zu CoA transferiert wird.
Wichtige Punkte zu Stoffwechselwegen und klinischen Krankheiten
Der Austausch mit anderen Hauptpfaden erfolgt mit G6P, F6P, DHAP, Pyruvat und Acetyl-CoA. Pyruvatkinase-Defizite erzeugen hämolytische Anämie als Folge niedriger intrazellulärer ATP-Konzentrationen.
der andere Beitrag
Karzinogenese (Tumorbildung)
https://www.sciencedirect.com/science/article/pii/B9780080468846014093
Bioverfügbarkeit und Stoffwechsel
Arsenit (Arsen III) und Arsenat (Arsen V) sind die häufigsten Formen von anorganischem Arsen, auf die der Mensch in natürlicher Umgebung stößt: Sie lecken aus dem Boden in Trinkwasser. Arsen ist natürlicherweise in Böden vorhanden und seine Hintergrundkonzentrationen liegen zwischen 0,2 und 40 mg / kg, übersteigen aber in Nordamerika nur selten 15 mg / kg (Pouschat und Zagury 2006). Unter den Elementen der Erdkruste steht es an 20. Stelle, im Meerwasser an 14. und im menschlichen Körper an 12. Stelle.
Organische Arsenverbindungen, unabhängig von der Form, wie sie in Lebensmitteln vorkommen, und anorganischen Arsenverbindungen, die in Wasser, Getränken, Pharmazeutika und mit Pestiziden behandelten oder industriell verschmutzten Kulturen vorkommen, werden vom Gastrointestinal (GI.) Leicht resorbiert (90–95%) ) Traktat. Die langzeitige niedrige Exposition gegenüber anorganischen Arsenstoffen, die in vielen Wasserquellen der Welt und ihren Sedimenten zu finden ist, ist die Ursache für die derzeit am häufigsten auftretende Gesundheitskrise, die heute mit Arsen-Toxizität verbunden ist. In Westbengalen, Indien und Südbangladesch sind über 100 Millionen Menschen Trinkwasser mit einem hohen Arsengehalt von 1 mg / l oder mehr ausgesetzt. Die US-amerikanische Umweltschutzbehörde EPA (Environmental Protection Agency, EPA) hat den zulässigen Arsengehalt von Trinkwasser in den Vereinigten Staaten in 2006 auf 10 μg l − 1 gesenkt. Weitere Regionen mit erhöhtem Arsengehalt im Trinkwasser sind Taiwan, China, Japan, Neuseeland , Argentinien, Chile, Russland und Kanada.
Ein wichtiger Gesichtspunkt bei der Risikobewertung, der mit der Arsenexposition beim Menschen korreliert ist, ist seine Bioverfügbarkeit und Biozugänglichkeit. Die Bioverfügbarkeit ist definiert als der Anteil an Verunreinigungen, der durch den GI-Trakt durch Arsen in den systemischen Kreislauf gelangt. Biozugänglichkeit ist definiert als der Anteil der im GI-System gelösten Kontaminanten, der möglicherweise für die Resorption verfügbar ist (Pouschat und Zagury 2006). Die Biozugänglichkeit hängt im Wesentlichen von Arsen ab von der Form von Arsen, das in den GI-Trakt gelangt. Nach Resorption durch das Darmepithel und Transport in das Blut wird Arsen durch Erythrozyten gebunden und mit sehr hoher Geschwindigkeit aus dem Blut entfernt. Lymphozyten nehmen auch Arsen auf und reduzieren das Arsenat zu Arsenit. Durch das Blut wird Arsen transportiert und an die Niere, Leber, Milz, Haut, Haare und Nägel verteilt.
Die Aufnahme in Zellen kann durch Säuger-Aquaglyceroporin-Kanäle wie AQP7 und AQP9 von Menschen und Ratten vermittelt werden. Kürzlich wurde entdeckt, dass der Glucosetransporter Isoform 1 (GLUT1), eine Säuger-Hexose-Permease, die mit den Hefe-Hxt-Permeasen homolog ist, den Transport von Arsentrioxid und MMA (III) erleichtert (Liu et al. 2006). Arsenat dringt durch das Phosphatträgersystem in die Zelle ein. Es kann mit Phosphat um die Bindung an Polyphosphate wie ADP konkurrieren (Nemeti und Gregus 2004).
Beim Menschen, wie bei den meisten Säugetieren, gibt es zwei Hauptreaktionen, die an der Biotransformation von Arsen beteiligt sind: die Reduktion von As (V) -Spezies (z. B. Arsenat) auf As (III) -Spezies (z. B. Arsenit) und die Methylierung (Aposhian et al. 2004) von anorganischen Arsenarten. Mindestens vier Enzyme im Menschen haben sich positiv auf Arsenat-reduzierende Aktivität getestet: Purinnucleosidphosphorylase (PNP) (Nemeti und Gregus 2004), Glyceraldehyd-3-phosphatdehydrogenase (GAPDH) (Gregus und Nemeti 2005), Glykogenphosphorylase (GP) ( Nemeti und Gregus 2007) und Monomethylarsenat (MMA (V)) -Reduktase (identisch mit humaner Glutathion-S-Transferase omega 1-1 (hGSTO1-1)) (Zakharyan et al. 2005). Arsen (+3-Oxidationsstufe) Methyltransferase verwendet S-Adenosylmethionin (SAM), Thioredoxin und ein Thiol, um Arsenit zu methylieren (Thomas et al. 2007). Es wird vermutet, dass der Weg vom anorganischen Arsen zu seinen methylierten Metaboliten diskrete Reduktionsschritte beinhaltet, die mit oxidativen Methylierungen abwechseln (El-Masri und Kenyon 2007; Thomas 2007) (Abbildung 2). Die Methylierung von Arsen wurde einst als Entgiftungsverfahren angesehen, weil es die Ausscheidung von Arsen erleichtert, und die fünfwertigen organischen Formen von Arsen (MMA (V) und DMA (V)) sind weniger toxisch als anorganisches Arsen. Dies wird jedoch nicht mehr angenommen, da eine Reihe von Spezies an Arsenmethylierung fehlt und anorganisches Arsen ausscheidet (Rossman 2007).
Über diese Phosphate wird ADP produziert und wenn es wirklich zutreffen sollte, dass der Arsenstoffwechsel uns vor gewissen Keimen schützt, wie Dr. Trarello mit seiner Arsentherapie beschreibt, dann finde ich das ist Bemerkenswert und zu beachten.
Das sage ich weil ich mir sicher bin, dass es Erreger gibt die in diesem Giftigen Umfeld sich aufhalten bzw. dieses Giftige Umfeld zu Ihrem Schutz aufbauen. Siehe dazu das Thema Muskelschmerzen oder bei mir noch diese Rückenschmerzen.
Der Stoffwechsel und die Methylisierung in den Pflanzen und in unserem Körper ist eigentlich geregelt. Mit geregelt meine ich, dass auch die Entgiftung dieser Stoffe geregelt von statten geht, wenn diese Stoffe dem natürlichen Ursprung entsprechen.
Das Zeigen die Anhänge.
- Arsen im Grundwasser
- Arsen-Methylisierung
- Arsen Bakterien
Gerade die Liste Arsen Bakterien finde ich doch sehr interessant und wichtig. Da doch gerade dort mehrere meiner pathogenen Keime aufgeführt sind. Und ich weis durch lesen im Forum, dass z.B. viele über Beschwerden und dann Klebsiella oxytoca genannt haben. Einen Bezug zum Candida-Pilz oder Galabrata wäre abzuklären, da ja Pilze Schwermetalle anziehen.
Durch die chemische Veränderung manipulieren wir jedoch diese Vorgänge und die Methylisierung läuft fehl.
Was mich jetzt einfach ganz gewaltig stört, dass ich feststellen musste, ich bin wohl nicht alleine von dem Erkrankungsproblem betroffen. Deswegen habe ich nie aufgebene danach zu suchen.
Ich hab auch bisher immer versucht alle ärztlichen Möglichkeiten zu nutzen, dass mir vielleicht jemand gesagt hätte, sie haben einen Gendefekt. Aber wie der Ablauf der Genberatung an der Uni Ulm verlaufen war und durchgeführt wurde, es war ein Witz sowohl personell von dem Arzt als auch Thematisch das Ergebnis. Okay wenn ich den Gendefekt kenne, oder ich weis das gibt es ein bestimmtes Phosphatproblem dann weis man das und befasst sich damit, was ist dazu bekannt, wie kann und muss ich mich verhalten bei der Ernährung, was sollte ich vermieden usw..
Aber so wie jetzt stellt sich ja keine Lösung dar. Es kann sein der Enzym-Schalter ist irreparabel geschädigt oder er ist reparabel vielleicht temporär. Sind die Keime, der Biofilm als Ursache zu sehen oder die Nahrungsmittel und welche. Ist die unterstützende Entgiftung nützlich oder produziert der Körper weiter immer weiter Arsen und lagert dieses ein.
Dazu sollte doch die Medizin da sein, mich in der Frage zu unterstützen. Muss ich denn deshalb Jahre im Internet danach suchen und mir den Ärger mit den Ärzten haben, weil ich vielleicht einen Ansatz im Arztgespräch einbringe.
Oder muss ich hunderte Nahrungsmittel und die sich ständig verändernden Herstellungsprodukte durchtesten, nur um mich ernähren zu können. Es muss doch festzustellen sein, welches Phosphat/e ob chemisch, natürlich oder in Kombination mit Keimen diesen Fehler verursachen.
Nun musste ich feststellen, dass dieses Enzym-Hemmung von Glyceraldehyd-3-phosphatdehydrogenase (GAPDH) durch Schwermetalle bzw. Arsen zwar bekannt ist, aber es keine Prüfung in der medizinischen Diagnostik gibt. Jedenfalls habe ich noch nichts gefunden. Im EBM-Katalog ist es nicht als Parameter zur Abrechnung erfasst.
Die Umweltmedizin prüft bzw. kann die Stoffwechselstörung das Schlüsselenzym Glucose-6-phosphat-dehydrogenase überprüfen, denn die Zellen brauchen NADPH/H+. Mit Vitamin C könnte man hier Einfluss nehmen.
Deshalb, wieso sollte ich jetzt viel Geld ausgeben für eine Behandlung die die Ursache nicht trifft. Diese 50:50 ärztlichen Behandlungen stellen mich nicht zufrieden.
Will mal noch zwei Beiträge zum Thema Arsen in Abstracten-Form einbringen.
Glykolyse und Pyruvatoxidation
https://www.sciencedirect.com/science/article/pii/B9780323074469000064
Arsenat- und Arsenitvergiftung
Arsenatvergiftung ist auf die Entkopplung der Phosphorylierung auf Substratebene durch G3P-Dehydrogenase zurückzuführen. Arsenat ist ein strukturelles Analogon des Phosphats und wird in 3PG eingebaut, um ein instabiles gemischtes Anhydrid zu bilden. Das Endergebnis ist die Freisetzung von Arsenat ohne Bildung von ATP. Dadurch wird der Nettogewinn von ATP durch anaerobe Glykolyse eliminiert und ist daher für den RBC am schädlichsten.
Aerobe Zellen sind betroffen, wenn Arsenat während der oxidativen Phosphorylierung mit der anschließenden spontanen Hydrolyse in ATP eingebaut wird, um ADP und freies Arsenat zu erzeugen. In beiden Fällen wird auch die mit der ATP-Hydrolyse verbundene Wärme freigesetzt.
Arsenitvergiftung ist auf die kovalente Reaktion von Arsenit mit Liponsäure zurückzuführen, wodurch verhindert wird, dass die Hydroxyethylgruppe von Thiamin zu CoA transferiert wird.
Wichtige Punkte zu Stoffwechselwegen und klinischen Krankheiten
Der Austausch mit anderen Hauptpfaden erfolgt mit G6P, F6P, DHAP, Pyruvat und Acetyl-CoA. Pyruvatkinase-Defizite erzeugen hämolytische Anämie als Folge niedriger intrazellulärer ATP-Konzentrationen.
der andere Beitrag
Karzinogenese (Tumorbildung)
https://www.sciencedirect.com/science/article/pii/B9780080468846014093
Bioverfügbarkeit und Stoffwechsel
Arsenit (Arsen III) und Arsenat (Arsen V) sind die häufigsten Formen von anorganischem Arsen, auf die der Mensch in natürlicher Umgebung stößt: Sie lecken aus dem Boden in Trinkwasser. Arsen ist natürlicherweise in Böden vorhanden und seine Hintergrundkonzentrationen liegen zwischen 0,2 und 40 mg / kg, übersteigen aber in Nordamerika nur selten 15 mg / kg (Pouschat und Zagury 2006). Unter den Elementen der Erdkruste steht es an 20. Stelle, im Meerwasser an 14. und im menschlichen Körper an 12. Stelle.
Organische Arsenverbindungen, unabhängig von der Form, wie sie in Lebensmitteln vorkommen, und anorganischen Arsenverbindungen, die in Wasser, Getränken, Pharmazeutika und mit Pestiziden behandelten oder industriell verschmutzten Kulturen vorkommen, werden vom Gastrointestinal (GI.) Leicht resorbiert (90–95%) ) Traktat. Die langzeitige niedrige Exposition gegenüber anorganischen Arsenstoffen, die in vielen Wasserquellen der Welt und ihren Sedimenten zu finden ist, ist die Ursache für die derzeit am häufigsten auftretende Gesundheitskrise, die heute mit Arsen-Toxizität verbunden ist. In Westbengalen, Indien und Südbangladesch sind über 100 Millionen Menschen Trinkwasser mit einem hohen Arsengehalt von 1 mg / l oder mehr ausgesetzt. Die US-amerikanische Umweltschutzbehörde EPA (Environmental Protection Agency, EPA) hat den zulässigen Arsengehalt von Trinkwasser in den Vereinigten Staaten in 2006 auf 10 μg l − 1 gesenkt. Weitere Regionen mit erhöhtem Arsengehalt im Trinkwasser sind Taiwan, China, Japan, Neuseeland , Argentinien, Chile, Russland und Kanada.
Ein wichtiger Gesichtspunkt bei der Risikobewertung, der mit der Arsenexposition beim Menschen korreliert ist, ist seine Bioverfügbarkeit und Biozugänglichkeit. Die Bioverfügbarkeit ist definiert als der Anteil an Verunreinigungen, der durch den GI-Trakt durch Arsen in den systemischen Kreislauf gelangt. Biozugänglichkeit ist definiert als der Anteil der im GI-System gelösten Kontaminanten, der möglicherweise für die Resorption verfügbar ist (Pouschat und Zagury 2006). Die Biozugänglichkeit hängt im Wesentlichen von Arsen ab von der Form von Arsen, das in den GI-Trakt gelangt. Nach Resorption durch das Darmepithel und Transport in das Blut wird Arsen durch Erythrozyten gebunden und mit sehr hoher Geschwindigkeit aus dem Blut entfernt. Lymphozyten nehmen auch Arsen auf und reduzieren das Arsenat zu Arsenit. Durch das Blut wird Arsen transportiert und an die Niere, Leber, Milz, Haut, Haare und Nägel verteilt.
Die Aufnahme in Zellen kann durch Säuger-Aquaglyceroporin-Kanäle wie AQP7 und AQP9 von Menschen und Ratten vermittelt werden. Kürzlich wurde entdeckt, dass der Glucosetransporter Isoform 1 (GLUT1), eine Säuger-Hexose-Permease, die mit den Hefe-Hxt-Permeasen homolog ist, den Transport von Arsentrioxid und MMA (III) erleichtert (Liu et al. 2006). Arsenat dringt durch das Phosphatträgersystem in die Zelle ein. Es kann mit Phosphat um die Bindung an Polyphosphate wie ADP konkurrieren (Nemeti und Gregus 2004).
Beim Menschen, wie bei den meisten Säugetieren, gibt es zwei Hauptreaktionen, die an der Biotransformation von Arsen beteiligt sind: die Reduktion von As (V) -Spezies (z. B. Arsenat) auf As (III) -Spezies (z. B. Arsenit) und die Methylierung (Aposhian et al. 2004) von anorganischen Arsenarten. Mindestens vier Enzyme im Menschen haben sich positiv auf Arsenat-reduzierende Aktivität getestet: Purinnucleosidphosphorylase (PNP) (Nemeti und Gregus 2004), Glyceraldehyd-3-phosphatdehydrogenase (GAPDH) (Gregus und Nemeti 2005), Glykogenphosphorylase (GP) ( Nemeti und Gregus 2007) und Monomethylarsenat (MMA (V)) -Reduktase (identisch mit humaner Glutathion-S-Transferase omega 1-1 (hGSTO1-1)) (Zakharyan et al. 2005). Arsen (+3-Oxidationsstufe) Methyltransferase verwendet S-Adenosylmethionin (SAM), Thioredoxin und ein Thiol, um Arsenit zu methylieren (Thomas et al. 2007). Es wird vermutet, dass der Weg vom anorganischen Arsen zu seinen methylierten Metaboliten diskrete Reduktionsschritte beinhaltet, die mit oxidativen Methylierungen abwechseln (El-Masri und Kenyon 2007; Thomas 2007) (Abbildung 2). Die Methylierung von Arsen wurde einst als Entgiftungsverfahren angesehen, weil es die Ausscheidung von Arsen erleichtert, und die fünfwertigen organischen Formen von Arsen (MMA (V) und DMA (V)) sind weniger toxisch als anorganisches Arsen. Dies wird jedoch nicht mehr angenommen, da eine Reihe von Spezies an Arsenmethylierung fehlt und anorganisches Arsen ausscheidet (Rossman 2007).
Anhänge
Zuletzt bearbeitet: